íííí2023─Û8È┬31╚ıú¼╩ðê÷▒O(ji¿ín)╣▄┐é¥Íò■═¼ç°╝Êðl(w¿¿i)╔·¢í┐Á╬»íóç°╝ÊÍðßt(y¿®)╦Ä¥ÍÍã¿▓ó┬ô(li¿ón)║¤░l(f¿í)▓╝íÂÈ╩ÈS▒ú¢í╩│ãÀ┬òÀQÁ─▒ú¢í╣ª─▄─┐õø ÀÃáIB(y¿úng)╦ÏÐa│õä®ú¿2023─Û░µú®íÀú¿ÊȤ┬║åÀQíÂ─┐õøíÀú®╝░┼õ╠Î╬─╝■íú┼õ╠Î╬─╝■Íðı²╩¢╠ß│÷îªË┌ÊÐ┼·£╩ÎóâÈÁ─«a(ch¿ún)ãÀÍðÎóâÈÎCò°í░ƒoËððºã┌║═ƒo«a(ch¿ún)ãÀ╝╝ðgʬþí▒Á─«a(ch¿ún)ãÀú¿ÊȤ┬║åÀQí░Ùpƒoí▒«a(ch¿ún)ãÀú®ı╣Ú_ôQÎC╣ñθíú
íííí2023─Û12È┬27╚ıú¼╩ðê÷▒O(ji¿ín)╣▄┐é¥Í░l(f¿í)▓╝╣½Ú_ı¸Ã¾íÂÈ┌«a(ch¿ún)È┌╩█í░Ùpƒoí▒▒ú¢í╩│ãÀ╝»ÍðôQÎCîÅ▓Úʬ³cú¿ı¸Ã¾ÊÔÊè©Õú®íÀú¿ÊȤ┬║åÀQí░ÊÔÊè©Õí▒ú®ÊÔÊèÁ─╣½©µíú2024─Û11È┬1╚ıú¼╩ðê÷▒O(ji¿ín)╣▄┐é¥Í░l(f¿í)▓╝íÂÈ┌«a(ch¿ún)È┌╩█í░ƒoËððºã┌║═ƒo«a(ch¿ún)ãÀ╝╝ðgʬþí▒▒ú¢í╩│ãÀ╝»ÍðôQÎCîÅ▓Úʬ³cíÀú¿ÊȤ┬║åÀQíÂôQÎCîÅ▓Úʬ³cíÀú®íú
íííí╩│ãÀ╗´░Ú¥W(w¿úng)┐é¢Y┴╦íÂôQÎCîÅ▓Úʬ³cíÀ¤Ó▒╚í░ÊÔÊè©Õí▒Á─͸ʬÎâ╗»ú¼╩ß└Ý┴╦ã¾ÿI(y¿¿)©¨ô■(j¿┤)íÂôQÎCîÅ▓Úʬ³cíÀÚ_ı╣í░Ùpƒoí▒«a(ch¿ún)ãÀôQÎCÁ─╣ñθʬ³cú¼ÊÈ╣®àó┐╝íú
Ê╗íóíÂôQÎCîÅ▓Úʬ³cíÀ¤Ó▒╚í░ÊÔÊè©Õí▒Á─͸ʬÎâ╗»
ííííú¿Ê╗ú®╩í╝ë¥Í╠ß│÷Á─ôQÎCÊÔÊè
íííííÂôQÎCîÅ▓Úʬ³cíÀÊÄ(gu¿®)¿║╦░l(f¿í)╔·«a(ch¿ún)ÈS┐╔Á─╩í╝ë¥Í╠ß│÷Á─ôQÎCÊÔÊèË╔ãõê¾╦═╩ðê÷▒O(ji¿ín)╣▄┐é¥Íú¼▓ó│¡╦═ÎóâÈ╚╦ú¼▓╗▓╔Ë├í░ÊÔÊè©Õí▒öMË╔ÎóâÈ╚╦¤‗╩ðê÷▒O(ji¿ín)╣▄┐é¥Í╠ߢ╗╩í╝ë¥Í│÷¥▀Á─ôQÎCÊÔÊèÁ─¢¿Îhú╗
ííííäh│²┴╦ÎóâÈ╚╦îª╩í╝ë¥ÍÊÔÊè╦¨©¢«a(ch¿ún)ãÀ╝╝ðgʬþ▀MðððÌËåòrÁ─┘Y┴¤Ê¬Ã¾ú¼▒Ý├¸╔Ûıê╚╦▓╗─▄îª╩í╝ë¥ÍÊÔÊè╦¨©¢«a(ch¿ún)ãÀ╝╝ðgʬþ▀MðððÌËåú╗
ííííäh│²┴╦í░ÊÔÊè©Õí▒Íðʬþ╩í╝ë¥Í│÷¥▀ÎóâÈ╚╦͸¾w┘Y┘|ÃÚør┤_ıJÊÔÊèÁ─ÊÄ(gu¿®)¿íú
ííííú¿Â■ú®╔Ûıê╚╦͸¾w┘Y┘|¤ÓÛP
íííííÂôQÎCîÅ▓Úʬ³cíÀäh│²┴╦í░ÊÔÊè©Õí▒îªË┌ÎóâÈ╚╦╠ÄË┌ÎóõNíóÁ§õNíó┴ð╚Ù¢ø(j¿®ng)áI«É│ú├¹õø╗‗▀`À¿╩ºð┼ã¾ÿI(y¿¿)├¹å╬Á╚«É│úÃÚð╬Á─ú¼ò║═ú╩▄└ÝÁ─ÊÄ(gu¿®)¿ú╗
ííííÈ÷╝Ë┴╦È¡ÎóâÈ╚╦ËðÂÓéÇ͸¾wÁ½▓┐ÀÍ͸¾wÎóõNòrú¼┤µ└m(x¿┤)ÎóâÈ╚╦È┌ôQÎCòræ¬╠ߢ╗Á─«a(ch¿ún)ãÀÎóâÈÎCò°Üwî┘ÖÓ┬ò├¸╗‗╔µ╝░Á─ÖÓ└¹┴xäıƒoáÄÎh│ðÍZò°╝░ıf├¸Á╚┘Y┴¤Ê¬Ã¾íú
ííííú¿╚²ú®È¡┴¤¤ÓÛP
ííííîªË┌È¡┴¤Ë├┴┐╗‗È¡┴¤ÀN¯ÉéÇöÁ(sh¿┤)Á╚│¼│÷¼F(xi¿ñn)ððÊÄ(gu¿®)¿Á─ÃÚørú¼íÂôQÎCîÅ▓Úʬ³cíÀÈ÷╝Ë┴╦Ê└ô■(j¿┤)«a(ch¿ún)ãÀÚLã┌╩│Ë├Á─░▓╚½ðÈıôÎC꾩µú¼¢ø(j¿®ng)Èu╣└ðÞʬ¢ÁÁ═È¡┴¤Ë├┴┐Á─ú¼È┌╩ıÁ¢▓╗ËÞ┼·£╩ôQÎCÊÔÊè║¾ú¼ÍÏð┬▀MððôQÎC╔Ûıêòrú¼┐╔├ÔË┌╠ß╣®öM¢ÁÁ═È¡┴¤Ë├┴┐║¾«a(ch¿ún)ãÀÁ─░▓╚½ðÈÈuârÈç‗×▓─┴¤ú¼Á½ðÞ╠ß╣®▒ú¢í╣ª─▄Èuâr▓─┴¤║═ðl(w¿¿i)╔·îWíóÀÇ(w¿ºn)¿ðÈíó╣ªðº│╔ÀÍ/ÿ╦Í¥ðÈ│╔ÀÍÖz£yÁ╚Èç‗×꾩µú¼ıôÎC«a(ch¿ún)ãÀ▒ú¢í╣ª─▄┼c┘|┴┐┐╔┐ÏðÈÁ─ÊÄ(gu¿®)¿íú
ííííîªË┌░┤ıı¼F(xi¿ñn)ððÊÄ(gu¿®)¿ı{ı¹«a(ch¿ún)ãÀ┼õÀ¢ú¿║¼╠µôQ╗‗╚Ñ│²È¡┴¤ú®Á─ú¼íÂôQÎCîÅ▓Úʬ³cíÀÈ÷╝Ë┴╦░┤ıı¼F(xi¿ñn)ððð┬«a(ch¿ún)ãÀÎóâÈʬþ╠ߢ╗«a(ch¿ún)ãÀ┼õÀ¢íó╔·«a(ch¿ún)╣ñ╦çíóÿ╦║×ıf├¸ò°ÿË©Õíó«a(ch¿ún)ãÀ╝╝ðgʬþÁ╚Ðð░l(f¿í)┘Y┴¤Á─ʬþíú
Â■íó░┤ııíÂôQÎCîÅ▓Úʬ³cíÀ▀Mððí░Ùpƒoí▒«a(ch¿ún)ãÀôQÎCòrÁ─╣ñθʬ³c
ííííú¿Ê╗ú®ôQÎCÀÂç·
íííí▀^Â╔ã┌ú¿2023─Û8È┬31╚ıã5─Ûâ╚ú®â╚È┌«a(ch¿ún)È┌╩█Á─ç°«a(ch¿ún)║═▀M┐┌í░Ùpƒoí▒«a(ch¿ún)ãÀíú
ííííú¿Â■ú®ôQÎC│╠ð‗
íííí1íóÎóâÈ╚╦¤‗╩ðê÷▒O(ji¿ín)╣▄┐é¥Í╠ß│÷Î⩳╔Ûıê
ííííÎóâÈ╚╦░┤ııíÂôQÎC║╦▓Úʬ³cíÀÁ─ÊÄ(gu¿®)¿£╩éõôQÎC┘Y┴¤ú¼▓ó¤‗╩ðê÷▒O(ji¿ín)╣▄┐é¥Í╠ß│÷Î⩳╔Ûıêú¼Î⩳ÎóâȯÉäe×Úí░Ùpƒoí▒ôQÎCíú
íííí2íó╩í╝ë¥Í│÷¥▀ôQÎCÊÔÊè
íííí╩í╝ë╩ðê÷▒O(ji¿ín)╣▄▓┐ÚT©¨ô■(j¿┤)«a(ch¿ún)ãÀîìÙH╔·«a(ch¿ún)Á─╝╝ðgʬþ║═▒O(ji¿ín)╣▄ÃÚørú¼Ê└ô■(j¿┤)¼F(xi¿ñn)ððÀ¿┬╔À¿ÊÄ(gu¿®)╠ß│÷«a(ch¿ún)ãÀôQÎCÊÔÊèú¼ê¾╦═╩ðê÷▒O(ji¿ín)╣▄┐é¥Íú¼▓ó│¡╦═ÎóâÈ╚╦íú
íííí3íó╝╝ðgîÅÈu
ííííîÅÈuÖCÿïú¿╩ðê÷▒O(ji¿ín)╣▄┐é¥Í╩│ãÀîÅÈuÍðð─ú®░┤ıı¼F(xi¿ñn)ððÀ¿┬╔À¿ÊÄ(gu¿®)ÿ╦£╩╝░ËðÛPÊÄ(gu¿®)¿Ú_ı╣ôQÎCîÅÈuú¼▓óîóîÅÈu¢Yıôê¾╦═╩ðê÷▒O(ji¿ín)╣▄┐é¥ÍîÅ┼·íú
íííí4íóððı■îÅ┼·
ííííÀ¹║¤Ê¬Ã¾Á─ú¼ôQ░l(f¿í)ð┬Á─ÎóâÈÎCò°ú¼ÎóâÈ╠û©³ð┬×Úí░ç°╩│¢íÎóG/J─Û┤·╠û+ð‗╠ûí▒ú¿ãõÍðí░─Û┤·╠û+ð‗╠ûí▒▓╗Îâú®ú¼ÎCò°éõÎóÖ┌ÿ╦ÎóÈ¡«a(ch¿ún)ãÀ├¹ÀQíóÈ¡«a(ch¿ún)ãÀÎóâÈ╠û╝░í░È¡ÎóâÈÎCò°ôQÎC║¾╩ºðºí▒íú
íííí▓╗À¹║¤Ê¬Ã¾Á─ú¼▓╗ËÞ┼·£╩ôQÎC╔ÛıêíúÎóâÈ╚╦┐╔Ê└ô■(j¿┤)ÊÄ(gu¿®)¿ʬþÍÏð┬╠ß│÷ôQÎC╔Ûıêíú
ííííôQ░l(f¿í)Á─ÎóâÈÎCò°╗‗▓╗ËÞÎóâÈøQ¿ò°ú¼═¼òr│¡╦═ÎóâÈ╚╦╦¨È┌ÁÏ║═║╦░l(f¿í)╔·«a(ch¿ún)ÈS┐╔Á─╩í╝ë╩ðê÷▒O(ji¿ín)╣▄▓┐ÚTíú
ííííú¿╚²ú®╣ñθʬ³c
íííí1íó╔Ûıê╚╦͸¾w┘Y┘|
ííííôQÎC╔Ûıê╚╦欫ö×ÚÎóâÈ╚╦íú▀M┐┌«a(ch¿ún)ãÀÁ─ÎóâÈ╚╦×Ú¥│═Ô╔·«a(ch¿ún)ÅS╔╠íú
íííí2íóôQÎCÊÔÊè│÷¥▀å╬╬╗
ííííí░Ùpƒoí▒«a(ch¿ún)ãÀôQÎCÊÔÊèË╔║╦░l(f¿í)╔·«a(ch¿ún)ÈS┐╔Á─╩í╝ë╩ðê÷▒O(ji¿ín)╣▄▓┐ÚT│÷¥▀ú¼╝┤«a(ch¿ún)ãÀîìÙH╔·«a(ch¿ún)ã¾ÿI(y¿¿)╦¨È┌ÁÏÁ─╩í╝ë¥Íú¼Â°▓╗╩ÃÎóâÈ╚╦╦¨È┌ÁÏÁ─╩í╝ë¥Ííú
íííí3íó«a(ch¿ún)ãÀ├¹ÀQ
íííí«a(ch¿ún)ãÀ├¹ÀQ欫öÀ¹║¤¼F(xi¿ñn)ððËðÛPÊÄ(gu¿®)¿íú▒ú┴¶«a(ch¿ún)ãÀÈ¡├¹ÀQÁ─ú¼└ÝË╔欫ö│õÀÍ║¤└Ýíú«a(ch¿ún)ãÀ├¹ÀQÁ─¼F(xi¿ñn)ððËðÛPÊÄ(gu¿®)¿ͩú║íÂ▒ú¢í╩│ãÀ├³├¹Í©─¤ú¿2019─Û░µú®íÀÁ┌╦─▓┐ÀÍÁ┌ú¿Â■ú®ùlÁ┌5┐¯ú¼í░Êн@Á├┼·£╩ÎCò°Á─▒ú¢í╩│ãÀú¼ãõ«a(ch¿ún)ãÀ├¹ÀQ│²▓╗À¹║¤▒¥ùl┐¯ÊÄ(gu¿®)¿═Ôú¼À¹║¤▒¥Í©─¤ãõ╦¹¤ÓÛPÊÄ(gu¿®)¿Á─ú¼╔Ûıê╚╦┐╔╠ß│÷│õÀÍ║¤└ÝÁ─└ÝË╔╔Ûıê▒ú┴¶È¡«a(ch¿ún)ãÀ├¹ÀQí▒íú
ííííı{ı¹«a(ch¿ún)ãÀ├¹ÀQÁ─ú¼┐╔È┌ð┬Á─«a(ch¿ún)ãÀ├¹ÀQ║¾└¿╠ûâ╚ÿ╦Îó«a(ch¿ún)ãÀÈ¡├¹ÀQú¼╩╣Ë├Í┴▒¥┤╬ôQ░l(f¿í)ÎCò°Ëððºã┌¢Y╩°íú
íííí4íó▀M┐┌í░Ùpƒoí▒«a(ch¿ún)ãÀôQÎC
ííííîªË┌È┌«a(ch¿ún)È┌╩█í░Ùpƒoí▒▀M┐┌«a(ch¿ún)ãÀú¼¤ÓÛP▓─┴¤À¹║¤íÂôQÎC║╦▓Úʬ³cíÀÊÄ(gu¿®)¿Á─ú¼ÎóâÈ╚╦░┤ııʬþÍ▒¢Ë╠ß│÷ôQÎC╔Ûıêíú¤Ó▒╚ç°«a(ch¿ún)í░Ùpƒoí▒«a(ch¿ún)ãÀôQÎC╠ߢ╗Á─┘Y┴¤ú¼▀Ç欫ö╠ߢ╗╬»═ðò°íó¥│═Ô╔·«a(ch¿ún)ÅS╔╠Á─┘Y┘|ÎC├¸╬─╝■íó╔·«a(ch¿ún)ã¾ÿI(y¿¿)┘|┴┐╣▄└ݾw¤ÁÎC├¸╬─╝■íó╔¤╩ðõN╩█Á─ÎC├¸╬─╝■íó¥│═ÔõN╩█╗‗▀M┐┌õN╩█Á─ίðíõN╩█░³ÐbîìÿËíóÎóâÈ╚╦ú¿¥│═Ô╔·«a(ch¿ún)ÅS╔╠ú®È┌╬Êç°│÷╚Ù¥│Öz‗×ÖzÊ▀▓┐ÚTÁ─éõ░©╗‗ÎóâÈð┼¤ó║═«a(ch¿ún)ãÀ▀M┐┌ð┼¤óíú
íííí5íóôQÎC╔µ╝░Öz£yÁ─ʬþ

ðí¢Yú║
íííííÂôQÎC║╦▓Úʬ³cíÀÍ╝È┌╝»ÍðÊÄ(gu¿®)ÀÂÈ┌«a(ch¿ún)È┌╩█í░Ùpƒoí▒«a(ch¿ún)ãÀÎóâÈÎCò°ú¼ÈO┴óÎóâÈÎCò°Ëððºã┌ú¼ÊÄ(gu¿®)ÀÂ▒ú¢í╣ª─▄┬òÀQú¼═Û╔ã«a(ch¿ún)ãÀÿ╦║×ıf├¸ò°ÿË©Õíó«a(ch¿ún)ãÀ╝╝ðgʬþ║═«a(ch¿ún)ãÀÖn░©ð┼¤óú¼ôQ░l(f¿í)▒ú¢í╩│ãÀÎóâÈÎCò°ú¼îì¼F(xi¿ñn)▒ú¢í╩│ãÀÎóâÈ┼c╔·«a(ch¿ún)ÈS┐╔íó▒O(ji¿ín)¢╣▄└ÝÒò¢Ëú¼┬õîì┬õ╝Ü╔·«a(ch¿ún)ã¾ÿI(y¿¿)͸¾wσ╚╬║═î┘ÁÏ▒O(ji¿ín)╣▄▓┐ÚT▒O(ji¿ín)╣▄σ╚╬íú
íííííÂôQÎC║╦▓Úʬ³cíÀÁ─░l(f¿í)▓╝ÊÔ╬ÂÍ°í░Ùpƒoí▒«a(ch¿ún)ãÀôQÎCÁ─ı²╩¢Ú_╩╝ú¼ãõÈö╝ÜÊÄ(gu¿®)¿┴╦í░Ùpƒoí▒«a(ch¿ún)ãÀôQÎCÁ─┴¸│╠╝░Î⩳╔Ûıê┘Y┴¤Ê¬Ã¾ú¼îª¤ÓÛPã¾ÿI(y¿¿)¥▀Ëð├¸┤_Á─Í©╩¥Î¸Ë├ú¼Ëð└¹Ë┌ı¹éÇððÿI(y¿¿)Á─ÊÄ(gu¿®)ÀÂ╝░┐╔│Í└m(x¿┤)░l(f¿í)ı╣íú
ííííÊÈ╔¤╩Ã╩│ãÀ╗´░Ú¥W(w¿úng)îªíÂôQÎC║╦▓Úʬ³cíÀÁ─╩ß└Ý║═┐é¢Yú¼╩│ãÀ╗´░Ú¥W(w¿úng)îóîª▒ú¢í╩│ãÀ╝░ãõ╦¹╠Ï╩Ô╩│ãÀ¤ÓÛPÁ─À¿ÊÄ(gu¿®)▀Mðð│Í└m(x¿┤)ðÈÁ─©³ð┬┼c¢ÔÎxú¼¥┤ıêã┌┤²íú
©¢╝■ú║
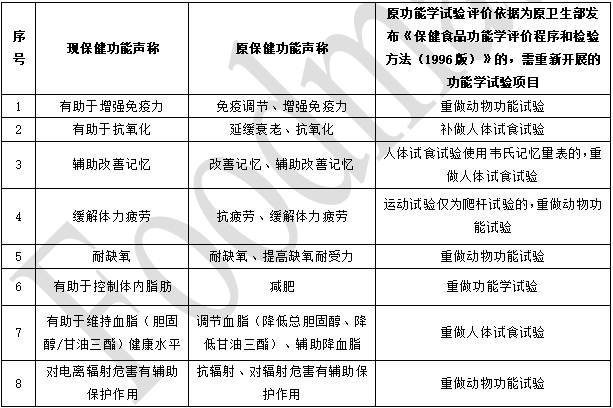
È¡╣ª─▄îWÈç‗×ÈuârÊ└ô■(j¿┤)×ÚÈ¡ðl(w¿¿i)╔·▓┐░l(f¿í)▓╝íÂ▒ú¢í╩│ãÀ╣ª─▄îWÈuâr│╠ð‗║═Öz‗×À¢À¿ú¿1996 ░µú®íÀÁ─8ÀN╣ª─▄Á─ð┬┼f▒ú¢í╣ª─▄┬òÀQîªæ¬ÛP¤Á║═╣ª─▄ÈuârÒò¢Ëʬþíú
©¢╝■ú║
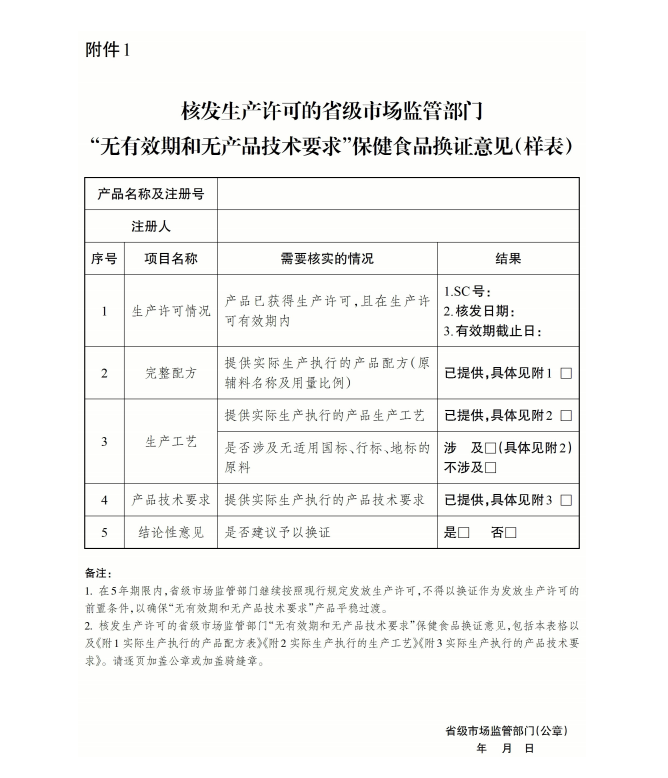
íííííÂÈ┌«a(ch¿ún)È┌╩█í░ƒoËððºã┌║═ƒo«a(ch¿ún)ãÀ╝╝ðgʬþí▒▒ú¢í╩│ãÀ╝»ÍðôQÎCîÅ▓Úʬ³cíÀÊТø(j¿®ng)2024─Û10È┬28╚ı╩ðê÷▒O(ji¿ín)╣▄┐é¥ÍÁ┌27┤╬¥Íäıò■Îh═¿▀^ú¼ ¼F(xi¿ñn)ËÞ╣½©µú¼ ÎÈ░l(f¿í)▓╝Í«╚ıã╩®ððíú
íííí╩ðê÷▒O(ji¿ín)╣▄┐é¥Í
íííí2024─Û10È┬30╚ı









 ╩ÍÖC░µ
╩ÍÖC░µ






![Ó]¤õ](https://img.foodmate.net/foodmate/img/zhiliangem.jpg)
